Periyodik tablo tarihi

Periyodik tablo, kimyasal elementlerin atom numarası, elektron konfigürasyonu ve yinelenen kimyasal özelliklerini baz alarak hazırlanmış bir düzenlemedir. Elementler artan atom numarasına göre sıralanmıştır. Tablonun standart formunda sistematik bir şekilde gösterilen elementlerle birlikte periyot adı verilen sıralar ve grup olarak adlandırılmış sütunlar bulunmaktadır.
Periyodik tablonun tarihi, bir asırdan uzun süredir devam eden kimyasal özellikleri anlamadaki gelişimi yansıtmaktadır. Tarihindeki en önemli olay, 1869 yılında Dimitri Mendeleyev’in[1] tabloyu yayınlamasıyla gerçekleşmiştir. Kendisi, daha önceden Antoine-Laurent de Lavoisier ve John Newlands gibi bilim adamları tarafından yapılmış olan keşiflerin üstüne yapmış olduğu katkılara rağmen, tablonun gelişiminde tek hak sahibi kişi olarak anılmaktadır.
Doğal formlarında bulunabilmeleri ve ilkel aletlerle kolay bir şekilde çıkarılabilmelerinden ötürü, birkaç fiziksel element (altın, gümüş ve bakır), eski uygarlık kalıntılarından anlaşıldığı üzere eskiden beri bilinmektedir.[2] Fakat, M.Ö. 330 yılı civarında var olan her şeyin belirli sayıda elementten meydana geldiği düşüncesi oluşmuş, ilk olarak Sicilyalı filozof Empedokles tarafından öne sürülmüş olan ve Yunan filozofu Aristoteles tarafından var olan her maddenin bir veya birden fazla kökün karışımından meydana geldiği düşüncesiyle desteklenmiştir. Bahsedilen kökler dört tane ve sonradan Platon tarafından element olarak nitelendirilmiş olan toprak, su, hava ve ateştir. Aristoteles ve Platon element konseptini oluşturmuş olsalar da, fikirleri maddenin doğasını anlama konusundaki gelişmelere katkı sağlamamıştır.
Aydınlanma Çağı
[değiştir | kaynağı değiştir]Hennig Brand
[değiştir | kaynağı değiştir]Periyodik tablonun tarihi aynı zamanda kimyasal elementlerin keşfinin de bir tarihidir. Tarihte ilk kez yeni bir element keşfeden kişi, aynı zamanda iflas etmiş bir tüccar olan Alman Hennig Brand’dır. Brand, efsanevi bir madde olan ve adi metalleri altına çevirdiği inanılan felsefe taşını keşfetmeye çalışmıştır. 1649 yılında, damıtılmış insan idrarıyla yaptığı deneyler sonucunda elde ettiği parlak beyaz maddeye fosfor ismini vermiştir.[3] Brand, yaptığı buluşu 1680 yılına kadar sır olarak saklamış, Robert Boyle fosforu yeniden keşfetmiş ve bulgularını yayınlamıştır. Fosforun keşfi, bir maddenin element olmasının ne anlama geldiği sorusunun açığa çıkmasına yardımcı olmuştur.
1661 yılında, Boyle bir elementi, “Bir kimyasal reaksiyonla kendinden daha basit bir malzemeye indirgenemeyen madde” olarak tanımlamıştır. Bu basit tanım atomaltı parçacıkların keşfine kadar, yaklaşık üç yüz yıl boyunca geçerli kabul edilmiş ve kullanılmıştır.
Antoine-Laurent de Lavoisier
[değiştir | kaynağı değiştir]
Lavoisier'in 1789 yılında yazdığı ve Robert Kerr tarafından İngilizceye çevrilen eseri Traité Élémentaire de Chimie (Kimya'nın Temel Bilimsel Eseri), kimya alanında yazılmış ilk modern ders kitabı olarak kabul edilmiştir. Kitabın içeriğinde Lavoisier'in daha küçük parçalara indirgenemeyeceğini düşündüğü ve günümüzde kullanılan element listesinin temelini oluşturan oksijen, nitrojen, hidrojen, fosfor, cıva, çinko ve sülfür listelenmiştir. Lavoisier'in listesi bahsedilen elementlerin yanı sıra, yaşadığı devirde madde olduğuna inanılan ışık ve ısıyı da kapsamaktadır. Lavoisier, maddeleri metal ve ametal olarak sınıflara ayırmıştır. Çoğu önde gelen kimyagerler, Lavoisier'in yeniliklerine karşı çıkmasına rağmen, the Elementary Treatise, genç nesli ikna edebilecek nitelikte yazılmış bir eserdir. Fakat, Lavoisier'in element tanımlamaları, elementleri sadece metaller ve ametaller olarak sınıflandırmasından ötürü eksik kabul edilir.
19. Yüzyıl
[değiştir | kaynağı değiştir]Johann Wolfgang Döbereiner
[değiştir | kaynağı değiştir]1817 yılında, Johann Wolfgang Döbereiner elementleri sınıflandırma konusunda yapılan ilk denemelerden birini formüle etmeye çalışmıştır. 1829 yılında, bazı benzer özellikleri taşıyan elementleri üçerli gruplar halinde ayırabileceğini anlamıştır. Bu gruplara üçlüler adını vermiştir. Döbereiner tarafından tanımlanan üçlülerin bazıları aşağıdaki gibidir;
- klor, brom ve iyot
- kalsiyum, stronsiyum ve baryum
- sülfür, selenyum ve tellür
- lityum, sodyum ve potasyum
Bütün üçlülerde, ortada bulunan elementin atom ağırlığı diğer iki elementin atom ağırlıklarının ortalamasına neredeyse eşittir.[4]
Alexandre Emile Béguyer de Chancourtois
[değiştir | kaynağı değiştir]Bir Fransız jeoloğu olan Alexandre-Émile Béguyer de Chancourtois, elementlerin periyodikliğini fark eden ilk kişiydi (Atom ağırlıklarına göre sıralandığında benzer özellikleri taşıyan elementlerin düzenli aralıklarla bulunması). 1862 yılında, Tellür elementinden esinlenerek oluşturduğu ve periyodik tablonun ilk formlarından sayılan VisTellurique (Tellür Sarmalı) adını verdiği tabloyu tasarladı.[5] Elementlerin artan atom ağırlıklarına göre spiral bir eğilimde bir silindir üzerinde bulunduğu bu sistemde, de Chancourtois benzer özellik taşıyan elementlerin dikey bir sırada yerleştiğini gözlemledi. Kendisinin 1863 yılındaki yayınında yer alan bir tablo elementlere ek olarak iyonları ve bileşikleri de kapsadı, fakat asıl olarak yayımladığı Comptes rendus de l'Académie des sciences (Bilim Akademisi Tutanakları) adlı makalesinde kimyasal terimlerden ziyade jeolojik terimleri kullandı ve bir diyagram kullanmadı. Sonuç olarak, de Chancourtois'in düşünceleri Dimitri Mendeleyev'in çalışmaları yayımlanana kadar dikkat çekmedi.[6]
John Newlands
[değiştir | kaynağı değiştir]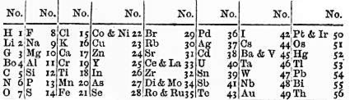
1864 yılında, İngiliz kimyager John Newlands bilinen 62 tane elementi fiziksel özelliklerine göre 7 farklı gruba ayırmıştır.[7][8]
Newlands birçok benzer elementin çiftler halinde bulunduğunu ve bunların kütle numaralarında 8'in katlarıyla farklılık gösterdiğini belirtmiş, elementlere ilk defa atom numaraları atayan bilim insanı olmuştur.[9] Chemisty News dergisinde yayınlanan, sekizlerin periyodikliğini müzikteki gamlara benzettiği ve adını “Oktavların Yasası” koyduğu çalışması dönemin bazı çağdaşları tarafından ciddiye alınmamıştır. 1 Mart 1866 tarihinde Chemistry Society (Kimya Topluluğu)’deki dersi yayımlanmamış, Topluluk ise buna neden olarak bu tarz teorik konuların tartışmaya açık olmasını göstermiştir.
Newlands’ın yaptığı analizler Chemistry Society (Kimya Topluluğu) tarafından ancak Mendeleyev’in çalışmaları fark edildikten sonra, altın madalya ile ödüllendirilmiştir. Sekizlerin periyodikliğinin öneminin kabulü ancak bir sonraki yüzyılda, Gilbert N.Lewis’in Değerlik Bağı Kuramı (1916) ve Langmuir’in Kimyasal Bağların Oktet Teorisi (1919) ile gerçekleşmiştir.[10][11] Newlands’in bilime olan katkısı 2008 yılında The Royal Chemistry Society (Kraliyet Kimya Topluluğu) tarafından “Kimyasal elementler için periyodik kanun’un kaşifi” sıfatıyla evine asılan mavi bir plaket ile kabul edilmiştir.[9]
Lothar Meyer
[değiştir | kaynağı değiştir]Mendeleyev ile tanışmamış olan bir Alman kimyageri olan Lothar Meyer'in de periyodik tablo konusunda çalışmaları olmuştur. Her ne kadar 1864'te Mendeleyev'den bağımsız hazırladığı çalışması yayımlanmış olsa da, az sayıda tarihçi Lothar Meyer'i periyodik tablonun ortak yaratıcılarından birisi olarak kabul etmektedir. Meyer'in tablosu, toplamda sadece 28 element içermiş ve elementleri atom numaralarına göre değil, değerliklerine göre sıralamıştır. Dolayısıyla, yeni elementleri tahmin etme ve atom ağırlıklarını düzeltme konusunda yetersiz kalmıştır. Mendeleyev'in bilinen elementlerden oluşan tabloyla beraber tabloyu tamamlamak adına yeni elementlerin varlığını tahmin etmesi ve bazı elementlerin atom ağırlıklarını düzeltmesini yayımlamasından yaklaşık 3 ay sonra, Meyer neredeyse aynı özelliklere sahip bir periyodik tablo yayımlamıştır.
Bazı bilim tarihçilerine göre, Mendeleyev ve Meyer'in periyodik tablonun ortak yaratıcısı olarak kabul edilmesi gerektiği belirtilirken, Mendeleyev'in keşfedilmemiş elementler konusundaki hassas tahminleri kendisinin periyodik tablonun keşfinde daha büyük bir pay sahibi olarak anılmasına sebebiyet vermiştir.
Dimitri Mendeleyev
[değiştir | kaynağı değiştir]


Rus kimyager Dimitri Mendeleyev günümüzde kullanılana en çok benzeyen periyodik tabloyu oluşturan ilk bilim adamıydı. Mendeleyev, elementleri atom numaralarının göreceli olarak molar ağırlıklarına karşılık gelecek şekilde sıraladı. Söylentilere göre, uzun tren yolculukları sırasında üzerlerinde bilinen elementlerle ilgili bilgiler bulunan kartlarla ‘Kimyasal iskambil oyunu’ oynamıştır.[12] 6 Mart 1869'da, Rus Kimyasal Topluluğu'na Elementlerin Atom Numaraları Özellikleri Arasındaki İlişki başlıklı resmi bir sunum yapıldı. Tablo, 1869 yılında ünlü olmayan bir Rus dergisinde yayımlanmış, ardından Zeitschrift für Chemie (Kimya Dergisi) adında bir Alman dergisinde yeniden yayımlanmıştır.[13] İçeriğinde Mendeleyev;
- Eğer elementler atom ağırlıklarına göre sıralanırsa özellikleri periyodik bir trend gösterir.
- Eğer elementlerin kimyasal özellikleri baz alınır ise, atom numaralarının birbirine yakın (Örn. Platin, İridyum, Osmiyum) veya düzenli aralıklarla artacak şekilde (Örn. K, Rb, Cs) olduğu gözlenir.
- Elementler veya element grupları atom ağırlıklarına göre sıralandığında, bahsedilen değerliklerine ve bir dereceye kadar ayırt edici kimyasal özelliklerine göre de sıralanmış olur; bu dizilim Li, Be, B, C, N, O ve F dizilerinde gözlenebilir.
- En geniş yayılma yüzeyine sahip olan elementler genellikle küçük atom ağırlıklarına sahiptirler.
- Molekül büyüklüğünün bir bileşiğin karakterini belirlediği gibi, atom ağırlığı da elementin karakterini belirler.
- Bilinmeyen bir sürü elementin keşfedileceğini düşünmeliyiz. Örneğin, atom ağırlıkları 65 ile 75 arasında olan ve alüminyum ile silikaya benzerlik gösterenler.
- Bazen, bir elementin atom ağırlığı sıralamada kendisiyle yan yana bulunan elementlerin varlığıyla düzeltilebilir. Dolayısıyla, tellürün atom ağırlığı 123 ile 126 arasında bulunmalı ve 128 olmamalıdır.
- Atom ağırlıkları baz alınarak bazı elementlerin karakteristik özellikleri tahmin edilebilir.
Mendeleyev'in Tablosu'nun Bilimsel Faydaları
- Mendeleyev'in yeni elementlerin keşfedileceğini tahmin etmesini sağladı ve keşfedilecek olan eka-silikon (germanyum), eka-alüminyum (galyum) ve eka-boron (skandiyum) için tabloda boşluklar bıraktı. Dolayısıyla, periyodik tablonun düzeni bozulmamış oldu.
- Mendeleyev'in, tabloyu kullanarak, o zamanlar doğru kabul edilen bazı atom ağırlıklarının yanlış olduğuna dikkat çekmesine olanak verdi.
- Atom ağırlığına göre sıralamada değişime olanak sağladı.
Mendeleyev'in Tablosu'nun Eksiklikleri
- Tablo, soygazların varlığını tahmin etme konusunda eksik kalmıştır. Fakat, soygazlar ailesinin tamamı keşfedildiğinde Sir William Ramsay, tablonun yansıttığı temel kavramı bozmadan soygazları "Grup 0" olarak entegre edebilmiştir.
- Hidrojen tek bir konuma yerleştirilememiş, alternatif olarak alkali metaller, halojenler veya tablodan ayrı ve üstte olacak şekilde bor ve karbon arasına konumlandırılmıştır.[14]
William Odling
[değiştir | kaynağı değiştir]1864 yılında, İngiliz bir kimyager olan William Odling, Mendeleyev'in oluşturduğu tabloya fazlasıyla benzeyen bir periyodik tablo çizmiştir. Odling, tellür – iyot problemini aşmış ve bunun yanında Mendeleyev'in ilk denemesinde başaramadığı talyum, kurşun, cıva ve platini doğru gruplara yerleştirmiştir. Odling fazla itibar kazanamamıştır. Fakat, kendisinin Londra Kimya Topluluğu Yazmanı olarak, Newlands'in periyodik tablo konusunda yaptığı önceki çalışmalarının hiçe sayılmasında başrol oynadığından şüphelenilmektedir.
20.Yüzyıl
[değiştir | kaynağı değiştir]Henry Moseley
[değiştir | kaynağı değiştir]1914 yılında, Gelibolu'da çatışmada öldürülmeden bir sene önce, İngiliz fizikçi Henry Moseley, bir elementin atom numarası ile X-ışınları arasındaki ilişkiyi yakalamıştır. Sonrasında, periyodik tabloyu atom ağırlıklarına göre değil, çekirdek yüklerine göre sıralayıp periyodik tabloyu yeniden düzenlemiştir. Bu buluştan önce, atom numaraları bir elementin atom ağırlığına göre belirlenen sıralı rakamlar olarak kabul görmekteydi. Moseley'in buluşu atom numaralarının aslında deneysel ölçümlerle elde edilebileceğini göstermiş oldu.
X-ışınlarının dalga boylarını kullanan Moseley, Argonun (Atom numarası Z=18) atom ağırlığı 39.9 ile 39.1 ağırlığındaki potasyumdan (Atom numarası Z=19) fazla olmasına rağmen, önüne koymuştur. Bu yeni düzenlemeyle, soygaz olan argon ve alkali metal olan potasyum elementlerinin kimyasal özellikleri tutarlı hale gelmiştir. Benzer şekilde, Moseley nikelden önce kobaltı yerleştirmiş ve tellürün atom ağırlığını deneysel olarak gözden geçirmesine gerek kalmadan, Mendeleyev'in önermiş olduğu gibi, tellürün iyottan önce gelmesi gerektiğini belirtmiştir.
Moseley'in çalışmaları atom numarası 43 ile 61 arasında olan elementlerin eksik olduğuna dikkat çekmiştir. Bu aralıktaki elementler günümüzde göreceli olarak teknesyum ve prometyum olarak adlandırılmıştır.
Glenn T. Seaborg
[değiştir | kaynağı değiştir]1943 yılında Manhattan Projesi için yaptığı araştırmalar sırasında Glenn T. Seaborg, amerisyum ve küriyumu ayırma konusunda beklenmedik zorluklarla karşılaşmıştır. Seaborg bu elementlerin, kimyasal özelliklerinin beklenenden farklı olması sebebiyle, farklı bir seriye ait olabileceğinden şüphelenmiştir. 1945 yılında meslektaşlarının itirazlarına rağmen, Mendeleyev'in oluşturduğu tabloda köklü bir değişim önermiştir: aktinit dizisi.
Seaborg'un aktinitlerin, lantanitler gibi nadir toprak elementlerine benzerlik gösterdiği ve bir geçiş serisi oluşturduğunu öngören aktinit konseptindeki ağır elementlerin elektronik yapısı, günümüzde kabul görmüş ve periyodik tabloda yerini almıştır. Aktinit serisi periyodik tabloda F-bloğun (5f) ikinci sırasında yer almaktadır. Aktinit ve lantanit serilerinin ikisinde de içerilerinde bulunan bir elektron yörüngesi doldurulmaktadır. Aktinit serisi elementler aktinyumdan lavrensiyuma kadar olan elementlerdir. Seaborg'un aktinik serileri konusunda sonradan yaptığı özenli çalışmaları, teorik olarak transaktinik serilerinde 104'ten 121'e kadar olan bir ağır element serisi ve 122'den 153'e kadar olan bir süperaktinik serisi ortaya çıkarmıştır.
Dış bağlantılar
- Development of the periodic table (http://www.rsc.org/periodic-table/history/about13 Aralık 2018 tarihinde Wayback Machine sitesinde arşivlendi.) (part of a collection of pages that explores the periodic table and the elements) by the Royal Society of Chemistry (http://www.rsc.org/25 Nisan 2013 tarihinde Wayback Machine sitesinde arşivlendi.) (Periyodik tablonun gelişimi) (periyodik tabloyu ve elementleri keşfeden makale derlemelerinin bir kısmı)
- The path to the periodic table (http://www.chemheritage.org/22 Aralık 1996 tarihinde Wayback Machine sitesinde arşivlendi. EducationalServices/chemach/ppt/ppt.html) by the Chemical Heritage Foundation (http://www.chemheritage.org/22 Aralık 1996 tarihinde Wayback Machine sitesinde arşivlendi.) (Periyodik tabloya giden yol)
- Dr. Eric Scerri's web page (http://www.ericscerri.com/14 Ekim 2013 tarihinde Wayback Machine sitesinde arşivlendi.), which has links to interviews, lectures and articles on various aspects of the periodic system, including the history of the periodic table. (Dr. Eric Scerrinin web sayfası, periyodik tablonun tarihi dahil olmak üzere, web sayfasında röportajlara, derslere ve makalelere ulaşılabilir.)
- The Internet Database of Periodic Tables (http://www.meta-synthesis.com/webbook/35_pt/pt_database.php5 Aralık 2018 tarihinde Wayback Machine sitesinde arşivlendi.) - a large collection of periodic tables and periodic system formulations. (Periyodik tablonun internet veritabanı) (Periyodik tabloların ve periyodik sistem formülizasyonlarının büyük derlemesi)
Kaynakça
[değiştir | kaynağı değiştir]- ^ "IUPAC article on periodic table" [Periyodik tablo hakkında IUPAC makalesi]. 24 Ocak 2010 tarihinde kaynağından arşivlendi. Erişim tarihi: 22 Mayıs 2015.
- ^ Scerri, E. R. (2006). The Periodic Table: Its Story ad Its Significance (Periyodik Tablo: Hikayesi ve önemi); New York City, New York; Oxford University Press.
- ^ ""A Brief History of the Development of Periodic Table" (Periyodik Tablo'nun Gelişiminin Kısa bir Tarihi)". people.wou.edu. 9 Şubat 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 12 Mart 2024.
- ^ Leicester, Henry M. (1971). The Historical Background of Chemistry (Kimya'nın Tarihsel Arka Planı); New York City, New York; Dover Publications.
- ^ Académie des sciences (France) (1862). Comptes rendus Academie des sciences 0055 (Fransızca). Académie des sciences (France). gallica.bnf.fr/. s. 660.
- ^ Annales des Mines history page ([ölü/kırık bağlantı]
- ^ in a letter published in Chemistry News in February 1863, according to the Notable Names Data Base (http://www.nndb.com/people/480/000103171/) 1 Ekim 2012 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Newlands on classification of elements (Elementlerin sınıflandırılması üzerine Newlands'in görüşleri)(http://web.lemoyne.edu/~giunta/EA/NEWLANDSann.HTML 1 Ocak 2011 tarihinde Wayback Machine sitesinde arşivlendi.)
- ^ a b John Newlands, Chemistry Review (Kimya incelemesi), November 2003, s. 15-16
- ^ IrvingLangmuir,“The Structure of Atoms and the Octet Theory of Valence” (Atomların yapısı ve değerliklerin Oktet Teorisi), Proceedings of the National Academy of Science, Vol. V, 252, Letters (1919)–online at [1] (http://dbhs.wvusd.k12.ca.us/ 4 Nisan 2015 tarihinde Wayback Machine sitesinde arşivlendi. webdocs/ Chem-History/Langmuir-1919.html)
- ^ IrvingLangmuir,“The Arrangement of Electrons in Atoms and Molecules”(Atomlar ve Moleküllerin içindeki Elektronların Düzenlenmesi) ,Journal of the American Chemical Society, Vol. 41, No, 6, pg. 868 (June 1919) – makalenini başlangıcı ve sonu online erişilebilir: [2] (http://dbhs.wvusd.k12.ca.us/webdocs/Chem-History/Langmuir-1919b.html 10 Aralık 2008 tarihinde Wayback Machine sitesinde arşivlendi.); ortası kayıptır.
- ^ PhysicalScience, Holt Rinehart & Winston (January2004), s.302 ISBN 0-03-073168-2
- ^ Mendeleev, Dmitri (1869). "Ueberdie Beziehungender Eigenschaftenzuden Atomgewichtender Elemente" (https://archive.org/stream/zeitschriftfrch12unkngoog#page/n414/mode/2up). Zeitschrift für Chemie 12: 405– 406. Retrieved 29 November 2013.
- ^ "Arşivlenmiş kopya". 24 Eylül 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 22 Mayıs 2015.
