Otoimmün hastalık
Otoimmün hastalık, bir vücut kısmına anormal bir bağışıklık tepkisinden kaynaklanan bir durumdur.[1] En az 80 otoimmün hastalık türü tanımlanmış olup, bazı kanıtlar 100'den fazla türün olabileceğini düşündürmektedir.[2][3][4] Herhangi bir vücut parçası tutulabilir.[5] Semptomlar çeşitlidir ve genellikle hafif ila şiddetli arasında değişen ve geçici olabilen düşük dereceli ateş ve yorgun hissetmeyi içerir.[1]
Nedeni bilinmiyor.[5] Lupus gibi bazı otoimmün hastalıklar aile takip eder, bazı vakalar enfeksiyon veya diğer çevresel faktörler tarafından tetiklenebilir.[1] Genellikle otoimmün olarak kabul edilen bazı yaygın hastalıklar arasında çölyak hastalığı, diabetes mellitus tip 1, graves hastalığı, inflamatuar barsak hastalığı, multipl skleroz, alopesi areata, addison hastalığı, pernisiyöz anemi, sedef hastalığı, romatoid artrit ve sistemik lupus eritematozus yer alır.[1][6] Teşhisi belirlemek zor olabilir.[1]
Tedavi, durumun tipi ve ciddiyetine bağlıdır.[1] Steroid olmayan anti-enflamatuar ilaçlar (NSAID'ler) ve immünosupresanlar sıklıkla kullanılır.[1] Bazen intravenöz immünoglobulin de kullanılabilir.[7] Tedaviler semptomları genellikle iyileştirirken, tipik olarak hastalığı iyileştirmez.[1]
Amerika Birleşik Devletleri'nde yaklaşık 24 milyon (~%7,5) insan bir otoimmün hastalıktan etkileniyor.[1][5] Kadınlar erkeklerden daha sık etkilenir.[1] Genellikle yetişkinlik döneminde başlarlar.[1] İlk otoimmün hastalıklar 1900'lerin başında tanımlandı.[8]
Belirti ve bulgular
[değiştir | kaynağı değiştir]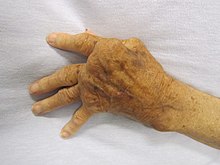
Seksenden fazla tipteki bazı otoimmün hastalıklar, benzer semptomlar gösterirken diğerleri, örneğin tip 1 diyabet, oldukça farklıdır.[9] Bu belirti ve semptomların varlığı ve ciddiyeti, meydana gelen otoimmün tepkinin yeri ve tipine bağlıdır. Bir kişi aynı anda birden fazla otoimmün hastalığa sahip olabilir ve her birinin semptomlarını gösterebilir. Sunulan belirti ve semptomlar ve hastalığın kendisi yaş, hormonlar, çevre ve diğer faktörlere bağlı olabilir.[10] Genel olarak, yaygın semptomlar şunlardır [11]
- yorgunluk
- düşük ateş
- genel olarak iyi hissetmemek (kırgınlık)
- kas ve eklem ağrıları
- döküntü.
Bu belirti ve semptomların görünümü değişebilir; yeniden ortaya çıkmalarına alevlenme denir.[11] Bu belirti ve semptomlar, test sonuçlarını destekleyerek tanıya yardımcı olabilir.[12]
Otoimmün hastalıklardan kan damarları, bağ dokuları, eklemler ve kaslar, kırmızı kan hücreleri, cilt ve endokrin bezleri (tiroid bezi ve pankreas gibi) dahil olmak üzere yaygın olarak etkilenen birkaç alan vardır.[11]
Bu hastalıklar, anormal bir bağışıklık tepkisinin olduğu dokularda hasar, organ büyümesi ve değişen fonksiyonlar dahil olmak üzere, onları otoimmün hastalıklar olarak karakterize eden patolojik etkilere sahip olma eğilimindedir.[11] Bazı hastalıklar sadece belirli organ ve dokuları etkilerken diğerleri sistemiktir ve vücuttaki birçok dokuyu etkiler. Belirti ve semptomlar, hastalık kategorisine bağlı olarak değişebilir.[13]
Kanserle ilişki
[değiştir | kaynağı değiştir]Bazı araştırmacılar, otoimmün hastalıklar ve kanser arasında genel bir korelasyon olduğunu, yani otoimmün hastalığa sahip olmanın belirli kanserleri geliştirme riskini artırdığını öne sürüyor.[14] Otoimmün hastalıklar çeşitli şekillerde iltihaplanmaya neden olur.[14] Kanser riski büyük ölçüde tüm otoimmün hastalıkların kanserle bağlantılı olan kronik enflamasyonu artırmasına bağlıdır.[14] Listede, çölyak hastalığı, enflamatuar barsak hastalığı (Crohn hastalığı ve ülseratif kolit), multipl skleroz, romatoid artrit ve sistemik lupus eritematozus dahil olmak üzere kanserle en sık bağlantılı bazı otoimmün hastalıklar yer almaktadır.[14]
Örnekler
[değiştir | kaynağı değiştir]Aşağıda otoimmün hastalıklara birkaç örnek verilmiştir. Daha ayrıntılı liste için otoimmün hastalıklar listesine bakın.
Çölyak hastalığı
[değiştir | kaynağı değiştir]Çölyak hastalığı, gastrointestinal ve lenfoproliferatif kanserlerle en güçlü ilişkileri sunar.[14] Çölyak hastalığında otoimmün reaksiyon, vücudun başlıca buğday, arpa ve çavdarda bulunan glütene karşı bağışıklık toleransını kaybetmesinden kaynaklanır.[14] Gastrointestinal kanal (yutulan glütenin sindirim sırasında geçeceği tüm alanlar) yemek borusu, mide, ince-kalın bağırsak, rektum ve anüsü içerdiğinden, bu, mide-bağırsak kanserlerinin artan riskini açıklar[14] Bir hasta diyetinden glüteni çıkarırsa, gastrointestinal kanser insidansı kısmen azaltılabilir veya ortadan kaldırılabilir.[14][15][16][17][18] Ek olarak, çölyak hastalığı lenfoproliferatif kanserler ile ilişkilidir.[14]
Enflamatuar barsak hastalığı
[değiştir | kaynağı değiştir]İnflamatuar barsak hastalığı, gastrointestinal sistem kanserleri ve bazı lenfoproliferatif kanserler ile ilişkilidir.[14] Crohn hastalığı veya ülseratif kolit olarak kategorize edilebilir.[14] Her iki durumda da, IBD'li bireyler, bağırsak mikrobiyomunda bulunan normal bakterilere karşı bağışıklık toleransını kaybeder.[14] Bağışıklık sistemi bakterilere saldırır ve kronik enflamasyonu indükler.[14]
Multipl skleroz
[değiştir | kaynağı değiştir]Multipl skleroz, başta beyin olmak üzere merkezi sinir sistemi kanseri riskinin artması, ancak genel kanser riskinin azalmasıyla ilişkilidir.[14] Multipl skleroz, spesifik bir bağışıklık hücresi türü olan T hücrelerinin beyin nöronlarındaki miyelin kılıfına saldırdığı nörodejeneratif bir hastalıktır.[19] Bu, sinir sistemi işlevini azaltır, enflamasyona ve ardından beyin kanserine neden olur.[14]
Romatizmal eklem iltihabı
[değiştir | kaynağı değiştir]Romatoid artrit, lenfoproliferatif kanserlerin yanı sıra vücuttaki fokal kanserlerle hafif, ancak önemli ilişkiler sunar.[14] Romatoid artritte, vücudun eklem ve kıkırdaklarını oluşturan hücreler lokal iltihaplanmaya neden olur.[14] Ek olarak, bağışıklık sisteminin kronik enflamasyonu ve aşırı aktivasyonu, diğer hücrelerin daha fazla habis dönüşümünü destekleyen bir ortam yaratır. Bu, akciğer ve deri kanseri ile olan ilişkileri ve ayrıca eklem iltihabından doğrudan etkilenmeyen diğer hematolojik kanser riskindeki artışı açıklayabilir.[20][21]
Sistemik lupus eritematoz
[değiştir | kaynağı değiştir]Sistemik lupus eritematozus vücuttaki fokal ve lenfoproliferatif kanserler ile ilişkilidir.[14] SLE çoklu organ sistemlerini etkiler ve yaygın bir immün tolerans kaybı ile karakterizedir.[22] Vücuttaki kronik iltihap, sistemik ve lenfoproliferatif kanser riskinin artmasına katkıda bulunan diğer hücrelerin habis dönüşümünü teşvik eder.[14] Tersine, sistemik lupus eritematozus bazı kanserlerde azalma ile ilişkilidir. Bu, en iyi şekilde bu alanlarda artan immün gözetim ile açıklanır, ancak bunun mekanizması tam olarak anlaşılamamıştır.[14]
Aplastik anemi
[değiştir | kaynağı değiştir]Aplastik anemide vücut yeterli sayıda kan hücresi üretemez. Kan hücreleri, kök hücreler tarafından kemik iliğinde üretilir. Aplastik anemi, tüm kan hücresi türlerinin eksikliğine neden olur: kırmızı, beyaz kan hücreleri ve trombositler.
Nedenler
[değiştir | kaynağı değiştir]Nedeni bilinmiyor.[5] Lupus gibi bazı otoimmün hastalıklar aileden geçer ve bazı vakalar enfeksiyonlar veya diğer çevresel faktörler tarafından tetiklenebilir.[1] 100'den fazla otoimmün hastalık vardır.[23] Otoimmün olduğu kabul edilen bazı yaygın hastalıklar arasında çölyak hastalığı, diabetes mellitus tip 1, Graves hastalığı, inflamatuar barsak hastalığı, multipl skleroz, sedef hastalığı, romatoid artrit ve sistemik lupus eritematozus yer alır.[1][6]
Genetik ve evrimsel seçilim
[değiştir | kaynağı değiştir]Tip 1 diyabet ve Romatoid artrit gibi hastalıklardan[24] sorumlu olabilecek genetik varyantları belirlemek için genom çapında ilişkilendirme çalışmaları (GWAS) yapıldı.[25]
İkiz çalışmalarında, otoimmün hastalıklar, çift yumurta ikizlerine kıyasla tek yumurta ikizleri arasında daha yüksek uyum oranı göstermektedir, örneğin multipl sklerozda %6'ya karşı %35.[26]
Ayrıca, enfeksiyona yatkınlığımız ile otoimmün hastalıklardan kaçınma becerimiz arasında bir denge sağlayan bazı genlerin evrim sırasında seçildiğine dair artan kanıtlar var. Örneğin, ERAP2 genindeki varyantlar, otoimmünite (pozitif seçilim) riskini artırmalarına rağmen enfeksiyona karşı bir miktar direnç sağlar. Buna karşılık, TYK2 genindeki varyantlar, otoimmün hastalıklara karşı koruma sağlar, ancak enfeksiyon riskini artırır (negatif seçim). Bu, enfeksiyon direncinin faydalarının otoimmün hastalık riskinden daha ağır bastığını düşündürmektedir ki bu, insanlık tarihinin büyük bölümünde yüksek enfeksiyon riski göz önüne alındığında şaşırtıcı değildir.[27]
Diğer örnekler
- Tip 1 diyabet, pankreas β hücrelerinin bağışıklık sistemi tarafından yok edildiği bir durumdur.[28] Pankreasta insülin üretimine aracılık eden gen (INS) mutasyona uğrar.[28] INS geni, 11p15.5 kromozomunun kısa kolunda, tirozin hidroksilaz ve insülin benzeri büyüme faktörü II genleri arasında bulunur.[29] 11. kromozoma ek olarak, tip 1 diyabetin genetik bir belirleyicisi, 6p21 kromozomu üzerinde yer alan ve majör histokompatibilite kompleksi (MHC) adı verilen bir lokustur.[25]
- Romatoid artrit : Bu durum için tam bir genetik haritalama olmamasına rağmen, birkaç genin RA'ya neden olabileceği düşünülmektedir. İnsan bağışıklık sistemini etkileyen genler, bir TNF reseptörü ile ilişkili faktör 1 (TRAF1) içerir. Bu TRAF1, 9q33-34 kromozomunda bulunur.[30] Ek olarak, insan genomundaki B1 genleri, en yaygın olarak RA hastalarında görülen yüksek konsantrasyonda HLA-DRB1 alelleri içerir.[31] RA şiddeti, genom içindeki polimorfizmlerin bir sonucu olarak değişebilir.[31]
Çevresel faktörler
[değiştir | kaynağı değiştir]Bir dizi çevresel faktörün otoimmün hastalığın katalizörü ya gelişiminde doğrudan bir rolü olduğu kabul edilir. Mevcut araştırmalar, otoimmün hastalıkların yüzde yetmiş kadarının, olasılıkla kimyasallar, enfeksiyon, diyet ve bağırsak disbiyozu gibi çevresel faktörlerden kaynaklandığını "göstermektedir". Otoimmün hastalık başlangıcı kesin kanıtı olmayan için teorik bir küme tanımlanmıştır.[32]
- Çevresel tetikleyiciler
- Azaltılmış oral tolerans
- Bağırsak disbiyozu
- Artan bağırsak geçirgenliği
- Artan bağışıklık reaktivitesi
- Otoimmünite
Hidrazinler, saç boyaları, trikloretilen, tartrazinler, tehlikeli atıklar ve endüstriyel emisyonlar dahil olmak üzere kimyasal veya ilaçlar.[33]
UV radyasyonunun dermatomiyozit,[34] pestisitlerin romatoid artrit gelişiminde rol oynadığı,[35] ve D vitamininin yaşlı populasyonda bağışıklık işlev bozukluklarını önlemede bir anahtar olduğu bulunmuştur.[36] Enfeksiyöz ajanlar, otoimmün hastalıkların aktivasyonu için gerekli bir adım olan T hücresi aktivatörleri olarak kabul edilir. Bu mekanizmalar nispeten bilinmemekte, ancak Guillain-Barre sendromu ve romatizmal ateş gibi enfeksiyon tarafından tetiklenen otoimmün hastalıkları açıklamak için mevcut alternatif teorilerden biridir.[37] Büyük kohortların verilerine dayanarak, COVID-19'a neden olan SARS-CoV-2 enfeksiyonunun, yeni başlayan çeşitli otoimmün hastalıklar geliştirme riskinin önemli ölçüde artmasıyla bağlantılı olabileceğine dikkat edilmelidir.[38]
Patofizyoloji
[değiştir | kaynağı değiştir]İnsan bağışıklık sistemi bir protein aracılığı ile kendi kendine reaktif olabilen T ve B hücrelerini üretir, ancak bu hücreler genellikle ya bağışıklık sistemi içinde aktif hale gelmeden önce öldürülerek sessizce bir anerji durumuna yerleştirilir veya düzenleyici hücreler tarafından bağışıklık sistemi içindeki rollerinden çıkarılır. Bu mekanizmalar başarısız olduğunda, bağışıklık sistemi içinde kendi kendine tepki veren hücrelerden oluşan bir rezervuara sahip olmak mümkündür. Kendi kendine tepki veren T hücrelerinin oluşmasını önleme mekanizmaları, T hücresi olgun bir bağışıklık hücresine dönüşürken timus içindeki negatif seçim süreciyle gerçekleşir.[kaynak belirtilmeli]
Campylobacter jejuni gibi bazı enfeksiyonlar, kendi moleküllerimize benzer antijenlere sahiptir. Bu durumda, C. jejuni'ye karşı normal bir bağışıklık tepkisi, periferik sinirlerin aksonlarını çevreleyen miyelin kılıfının gangliyositleri (yani, Guillain-Barré ) ile daha düşük bir dereceye kadar reaksiyona giren antikorların üretimi ile sonuçlanabilir. Otoimmün hastalıkların altında yatan patofizyolojinin anlaşılmasına hastalıklar arasında bir dereceye kadar genetik paylaşım tanımlayan genom çapında ilişkilendirme taramaları katkıda bulunurr.[39]
Öte yandan, otoimmünite, kendi kendine reaktif bağışıklık tepkisinin (örneğin, oto-antikorlar, kendi kendine reaktif T hücreleri), hasar veya hasarsız varlığıdır.[40] Otoantikorlar çoğu otoimmün bozukluğun ayırt edici özelliğidir.[41] Bu, belirli organlarla sınırlı (örn. otoimmün tiroiditte) olabileceği gibi farklı organları ilgilendiren belirli bir dokuyla ilgili olabilir. (örn. Hem akciğer hem de böbrekte bazal membranı etkileyebilen Goodpasture hastalığı).
Bir otoimmün hastalık durumunun nasıl ortaya çıktığına dair birçok farklı teori vardır.
Teşhis
[değiştir | kaynağı değiştir]Bir hastalığın otoimmün hastalık olarak kabul edilmesi için, Witebsky'nin varsayımlarına (ilk olarak 1957'de Ernest Witebsky ve meslektaşları tarafından formüle edilmiş ve 1994'te değiştirilmiştir) yanıt vermesi gerekir:[42][43]
- Hastalığa neden olan antikor veya hastalığa neden olan T lenfosit hücrelerinin transferinden doğrudan kanıt
- Deney hayvanlarında otoimmün hastalığın üremesine dayalı dolaylı kanıtlar
- Klinik ipuçlarından dolaylı kanıtlar
Erken otoimmün hastalığın belirtileri olan yorgunluk, ateş, halsizlik, eklem ağrısı ve kızarıklık gibi semptomlar etkilenen yer, hastalığa neden olan ajanlar ve bireyler için farklılık gösterdiğinden, doğru teşhis zordur.[11] Tipik olarak tanı, bir hastanın ailesinin genetik yatkınlık geçmişine bakılmasıyla başlar. Bu, çeşitli testlerle birleştirilir, çünkü hiçbir test tek başına bir otoimmün hastalığı tanımlayamaz.[33]
Antinükleer antikor
[değiştir | kaynağı değiştir]Vücut kendi dokularına saldırdığında üretilen ve antinükleer antikorlar olarak bilinen proteinleri tanımlamak için kullanılan bir testtir.[11][33] Çeşitli bozukluklarda pozitifleşebilir. Bu test, %95 oran ile sistemik lupus eritematozus teşhisinde en kullanışlı testtir.[44]
Tam kan sayımı
[değiştir | kaynağı değiştir]Kan hücrelerinin olgunluk seviyeleri, sayısı ve boyutu hakkında ölçümler yapan bir testtir.[11][33] Şunları içerir: kırmızı kan hücreleri, beyaz kan hücreleri, hemoglobin, hematokrit ve trombositler. Bu sayımlardaki artan veya azalan sayılara bağlı olarak, altta yatan tıbbi durumlar değerlendirilir; tipik olarak otoimmün hastalık, düşük beyaz küre sayısı (Lökopeni) ile temsil edilir. Doğru teşhis için daha ileri testlere ihtiyaç vardır.[45]
Kompleman
[değiştir | kaynağı değiştir]Kandaki bağışıklık sistemine ait kompleman adı verilen bir protein grubunun seviyelerini ölçmek için kullanılan bir testtir. Kompleman düşük seviyelerde bulunursa, bu bir hastalık belirtisidir.[11][33]
C-reaktif protein
[değiştir | kaynağı değiştir]Karaciğerde yapılan bir protein olan C-reaktif protein genellikle iltihaplanma ile artar ve otoimmün hastalıklarda yüksek olabilir.[11][33]
Eritrosit sedimantasyon hızı
[değiştir | kaynağı değiştir]Bu test, bir hastanın kan hücrelerinin bir test tüpüne inme hızını ölçer. Daha hızlı inişler, otoimmün hastalığın yaygın bir semptomu olan iltihaplanmayı gösterir.[33][11]
Bu testler, antikor anormallikleri ve iltihaplanmayı gösteriyorsa, mevcut otoimmün hastalığı belirlemek için başka testler yapılacaktır.[33]
Tedavi
[değiştir | kaynağı değiştir]Tedavi, durumun tipi ve ciddiyetine bağlıdır. Otoimmün hastalıkların çoğu kroniktir ve kesin bir tedavisi yoktur, ancak tedavi ile semptomlar hafifletilebilir ve kontrol altına alınabilir.[46] Standart tedavi şunları içerir:[11]
- Hastalık nedeniyle vücutta eksik olan vitamin veya hormon takviyeleri (insülin, vitamin B12, tiroid hormonu vb.) )
- Hastalık kanla ilgiliyse kan nakli
- Hastalık kemik, eklem veya kasları etkiliyorsa fizik tedavi
Ayrıca vücudun kendi dokularına karşı bağışıklık tepkisini azaltmak için bağışıklık bastırıcı ilaçlar verilir, örneğin:[47]
- İltihabı azaltmak için steroidal olmayan anti-enflamatuar ilaçlar (NSAID'ler)
- İltihabı azaltmak için glukokortikoidler
- Enflamatuar otoimmün tepkinin doku ve organlara zarar veren etkilerini azaltmak için hastalık modifiye edici anti-romatizmal ilaçlar (DMARD'lar)
İmmün baskılayıcılar genel bağışıklık tepkisini zayıflatır. Tedavi potansiyel olarak yaşamı tehdit edebilecek enfeksiyonlarla mücadele ile dengelenmelidir.[48]
Geleneksel olmayan tedaviler, geleneksel tedaviler başarısız olduğunda uygulanmak üzere geliştirilmekte ve kullanılmaktadır. Bu yöntemler vücuttaki patojenik hücrelerin aktivasyonunu bloke etmeyi veya değiştirmeyi amaçlar.[48][49] Bu tedaviler hasta için daha az toksik olmayı amaçlar ve daha spesifik hedefleri vardır.[49] Bu tür seçenekler şunları içerir:
- Proinflamatuar sitokinleri bloke etmek için kullanılabilen monoklonal antikorlar
- Bağışıklık sisteminin otoimmün hastalığa neden olan anormal hücreleri spesifik olarak hedeflemesine izin veren, antijene özgü immünoterapi.[49]
- Otoimmün cevaba yol açan yolu bloke etmeye yardımcı uyarıcı blokajı
- Otoimmün yanıtı baskılamak üzere özel düzenleyici T hücre tedavisi[48]
Epidemiyoloji
[değiştir | kaynağı değiştir]Otoimmün hastalıkların ABD prevalansına ilişkin ilk tahmin, 1997'de Jacobson ve diğerleri tarafından yayınlandı. 24 hastalık için tahminlerinin 279 milyonluk ABD nüfusunda 9 milyon civarında olduğunu bildirdiler.[50] Jacobson'ın çalışması 2012 yılında Hayter & Cook tarafından güncellendi.[51] Bu çalışma, listeyi 81 hastalığa genişleterek Rose & Bona[43] tarafından revize edilen Witebsky'nin varsayımlarını kullandı ve genel kümülatif ABD prevalansını %5,0, erkekler için %3,0 ve kadınlar için %7,1 olarak tahmin etti. Pek çok insanın birden fazla otoimmün hastalığa sahip olduğu gözlemini hesaba katan tahmini toplum yaygınlığı, erkeklerde %2,7 ve kadınlarda %6,4 olmak üzere genel olarak %4,5'tir.[51] 1980'lerden günümüze ABD'de yürütülen Ulusal Sağlık ve Beslenme İnceleme Araştırmaları, otoimmün hastalıklar için yaygın bir biyobelirteç olan antinükleer antikorlarda artış olduğunu göstermiştir. Bu durum, otoimmün hastalıklar için bir risk faktörü olarak çevre faktörlerinin etkisinin daha güçlü olduğuna işaret ederek son yıllarda otoimmün hastalıkların prevalansında bir artış olduğunu göstermektedir.[52]
Araştırmalar
[değiştir | kaynağı değiştir]Hem otoimmün hem de enflamatuar hastalıklarda, durum, insan adaptif veya doğuştan gelen bağışıklık sistemlerinin anormal reaksiyonları yoluyla ortaya çıkar. Otoimmünitede, hastanın bağışıklık sistemi vücudun kendi proteinlerine karşı aktive olur. Kronik enflamatuar hastalıklarda, nötrofiller ve diğer lökositler yapısal olarak sitokinler ve kemokinler tarafından alınır ve doku hasarına neden olur.
Anti-inflamatuar genlerin aktivasyonu ve inflamatuar genlerin immün hücrelerde baskılanması yoluyla enflamasyonun hafifletilmesi umut verici bir terapötik yaklaşımdır.[53][54][55] Otoantikorların üretimi bir kez başlatıldıktan sonra, otoantikorların kendi üretimlerini sürdürme kapasitesine sahip olduğuna dair çok sayıda kanıt vardır.[56]
Kök hücre tedavisi
[değiştir | kaynağı değiştir]Kök hücre nakli üzerinde çalışılmaktadır ve bazı durumlarda ümit verici sonuçlar vermiştir.[57]
Tip 1 diyabette yok olan pankreatik β hücrelerinin yerini alacak hücreler için tıbbi denemeler devam etmektedir.[58]
Değiştirilmiş glikan teorisi
[değiştir | kaynağı değiştir]Bu teoriye göre, bağışıklık tepkisinin efektör işlevine, bağışıklık sisteminin hücreleri ve hümoral bileşenleri tarafından sergilenen glikanlar (polisakkaritler) aracılık eder. Otoimmün bireyler, glikosilasyon profillerinde, proinflamatuar bir bağışıklık tepkisinin tercih edileceği şekilde değişikliklere sahiptir. Ayrıca, bireysel otoimmün hastalıkların benzersiz glikan imzalarına sahip olacağı varsayılmaktadır.[59]
Hijyen hipotezi
[değiştir | kaynağı değiştir]Hijyen hipotezine göre, yüksek düzeyde temizlik, çocukları geçmişe göre daha az antijene maruz bırakarak bağışıklık sistemlerinin aşırı tepki vermesi ve kendi dokularını yabancı olarak tanımlamasıyla otoimmün veya astım gibi alerjik durumlara neden olmaktadır.[60]
Bağışıklık yanıtında D vitamini
[değiştir | kaynağı değiştir]D vitamini, adaptif ve doğuştan gelen bağışıklığa yardımcı olan bir bağışıklık düzenleyici olarak biliniyor.[61][62] Kalıtsal veya çevresel etkilerden kaynaklanan D vitamini eksikliği, daha zayıf bir bağışıklık tepkisine yol açabileceği gibi otoimmün hastalıkların gelişimine katkıda bulunan bir faktör olarak da görülüyor.[62] D vitamini mevcut olduğunda, D vitamini yanıt elementleri (VDRE), model tanıma reseptörleri (PRR) yanıtları ve bu yanıtlarla ilişkili genler yoluyla kodlanır ve ifade edilir.[61] İfade edilen spesifik DNA hedef dizisi, 1,25-(OH)2D3 olarak bilinir.[61] 1,25-(OH)2D3'ün ifadesi makrofajlar, dendritik hücreler, T ve B-hücreleri tarafından indüklenebilir.[61] 1,25-(OH)2D3 varlığında, bağışıklık sisteminin inflamatuar sitokin üretimi baskılanır ve daha tolerojenik düzenleyici T-hücreleri ifade edilir.[61] Nedeni, D vitamininin hücre olgunlaşması, özellikle T hücreleri ve bunların fenotip ekspresyonu üzerindeki etkisidir.[61] 1,25-(OH)2D3 ekspresyonunun olmaması, daha az toleranslı düzenleyici T-hücrelerine, antijenlerin daha az toleranslı T-hücrelerine daha büyük sunumuna ve artmış inflamatuar yanıta yol açabilir.[61]
Ayrıca bakınız
[değiştir | kaynağı değiştir]- Otoimmün hastalıklar listesi
Kaynakça
[değiştir | kaynağı değiştir]- ^ a b c d e f g h i j k l m "Autoimmune diseases fact sheet". U.S. Department of Health and Human Services. 16 Temmuz 2012. 5 Ekim 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Ekim 2016.
- ^ "List of Autoimmune Diseases". Autoimmune Registry Inc. (İngilizce). 21 Kasım 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Haziran 2022.
- ^ Angum (13 Mayıs 2020). "The Prevalence of Autoimmune Disorders in Women: A Narrative Review". Cureus (İngilizce). 12 (5): e8094. doi:10.7759/cureus.8094. ISSN 2168-8184. PMC 7292717 $2. PMID 32542149. 15 Nisan 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 30 Mayıs 2023.
- ^ "Assessment of NIH Research on Autoimmune Diseases". www.nationalacademies.org. 2 Kasım 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 13 Haziran 2022.
- ^ a b c d Women's Health Across the Lifespan: A Pharmacotherapeutic Approach (İngilizce). ASHP. 2010. s. 579. ISBN 978-1-58528-194-7. 8 Eylül 2017 tarihinde kaynağından arşivlendi.
- ^ a b "The search for the target antigens of multiple sclerosis, part 1: autoreactive CD4+ T lymphocytes as pathogenic effectors and therapeutic targets". The Lancet Neurology. 15 (2): 198-209. February 2016. doi:10.1016/S1474-4422(15)00334-8. PMID 26724103.
- ^ "Update on intravenous immunoglobulins (IVIg) mechanisms of action and off- label use in autoimmune diseases". Current Pharmaceutical Design. 17 (29): 3166-75. 2011. doi:10.2174/138161211798157540. PMID 21864262.
- ^ Ananthanarayan and Paniker's Textbook of Microbiology (İngilizce). Orient Blackswan. 2005. s. 169. ISBN 9788125028086. 8 Eylül 2017 tarihinde kaynağından arşivlendi.
- ^ "Autoimmune Diseases: Types, Symptoms, Causes and More". Healthline. 26 Mart 2019. 9 Ekim 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Kasım 2020. Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Introduction to immunology and autoimmunity". Environmental Health Perspectives. 107 Suppl 5 (suppl 5): 661-5. October 1999. doi:10.1289/ehp.99107s5661. PMC 1566249 $2. PMID 10502528.
- ^ a b c d e f g h i j k MedlinePlus Medical Encyclopedia. Kaynak hatası: Geçersiz
<ref>etiketi: "MedLinePlus_Autoimmune_disorders" adı farklı içerikte birden fazla tanımlanmış (Bkz: Kaynak gösterme) - ^ National Research Council (US) Subcommittee on Immunotoxicology (1992). Autoimmune Diseases (İngilizce). National Academies Press (US). 7 Nisan 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 30 Mayıs 2023.
- ^ "Human autoimmune diseases: a comprehensive update". Journal of Internal Medicine. 278 (4): 369-95. October 2015. doi:10.1111/joim.12395. PMID 26212387.
- ^ a b c d e f g h i j k l m n o p q r s t "Multiple associations between a broad spectrum of autoimmune diseases, chronic inflammatory diseases and cancer". Anticancer Research. 32 (4): 1119-36. April 2012. PMC 3349285 $2. PMID 22493341.
- ^ "Celiac disease: from oral tolerance to intestinal inflammation, autoimmunity and lymphomagenesis". Mucosal Immunology. 2 (1): 8-23. January 2009. doi:10.1038/mi.2008.75. PMID 19079330.
- ^ "Risk of malignancy in patients with celiac disease". The American Journal of Medicine. 115 (3): 191-5. August 2003. doi:10.1016/s0002-9343(03)00302-4. PMID 12935825.
- ^ "Papillary cancer of thyroid in celiac disease". Journal of Clinical Gastroenterology. 45 (5): e44-6. 2011. doi:10.1097/mcg.0b013e3181ea11cb. PMID 20697293.
- ^ "Association of celiac disease and intestinal lymphomas and other cancers". Gastroenterology. 128 (4 Suppl 1): S79-86. April 2005. doi:10.1053/j.gastro.2005.02.027. PMID 15825131.
- ^ "Multiple sclerosis--the plaque and its pathogenesis". The New England Journal of Medicine. 354 (9): 942-55. March 2006. doi:10.1056/nejmra052130. PMID 16510748.
- ^ "Clinical Features of Rheumatoid Arthritis: Extra-Articular Manifestations". Rheumatoid Arthritis. Elsevier. 2009. ss. 62-67. doi:10.1016/b978-032305475-1.50014-8. ISBN 978-0-323-05475-1.
- ^ "Clinical aspects of rheumatoid arthritis". Pathophysiology. 12 (3): 153-65. October 2005. doi:10.1016/j.pathophys.2005.07.009. PMID 16125918.
- ^ "Systemic lupus erythematosus". The New England Journal of Medicine. 365 (22): 2110-21. December 2011. doi:10.1056/nejmra1100359. PMID 22129255.
- ^ "Autoimmune Disease List • AARDA". AARDA (İngilizce). 1 Haziran 2016. 23 Haziran 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 21 Mart 2019.
- ^ "Recent advances in the genetics of autoimmune disease". Annual Review of Immunology. 27: 363-91. 2009. doi:10.1146/annurev.immunol.021908.132653. PMC 2992886 $2. PMID 19302045.
- ^ a b "Recent acquisitions on the genetic basis of autoimmune disease". Frontiers in Bioscience: A Journal and Virtual Library. 13 (13): 4838-51. May 2008. doi:10.2741/3043. PMID 18508549.
- ^ Filippi (8 Kasım 2018). "Multiple sclerosis". Nature Reviews Disease Primers (İngilizce). 4 (1): 43. doi:10.1038/s41572-018-0041-4. ISSN 2056-676X. PMID 30410033. 6 Mayıs 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 31 Mayıs 2023.
- ^ Harroud (5 Mayıs 2023). "Common genetic factors among autoimmune diseases". Science (İngilizce). 380 (6644): 485-490. doi:10.1126/science.adg2992. ISSN 0036-8075. PMID 37141355. 17 Mayıs 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 31 Mayıs 2023.
- ^ a b "Mutations in the insulin gene can cause MODY and autoantibody-negative type 1 diabetes". Diabetes. 57 (4): 1131-5. April 2008. doi:10.2337/db07-1467. PMID 18192540.
- ^ "Human type 1 diabetes and the insulin gene: principles of mapping polygenes". Annual Review of Genetics. 30: 343-70. 1996. doi:10.1146/annurev.genet.30.1.343. PMID 8982458.
- ^ "A candidate gene approach identifies the TRAF1/C5 region as a risk factor for rheumatoid arthritis". PLOS Medicine. 4 (9): e278. September 2007. doi:10.1371/journal.pmed.0040278. PMC 1976626 $2. PMID 17880261.
- ^ a b "Correlation between disease phenotype and genetic heterogeneity in rheumatoid arthritis". The Journal of Clinical Investigation. 95 (5): 2120-6. May 1995. doi:10.1172/JCI117900. PMC 295811 $2. PMID 7738179.
- ^ "A Potential Link between Environmental Triggers and Autoimmunity". Autoimmune Diseases. 2014: 437231. 2014. doi:10.1155/2014/437231. PMC 3945069 $2. PMID 24688790.
- ^ a b c d e f g h "Autoimmune Diseases: Symptoms & Causes". Boston Children's Hospital. 7 Nisan 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Mart 2020.. Boston Children's Hospital. Archived from the original 7 Nisan 2021 tarihinde Wayback Machine sitesinde arşivlendi. on 7 April 2021. Retrieved 23 March 2020.
- ^ "Brief report: ultraviolet radiation exposure is associated with clinical and autoantibody phenotypes in juvenile myositis". Arthritis and Rheumatism. 65 (7): 1934-41. July 2013. doi:10.1002/art.37985. PMC 3727975 $2. PMID 23658122.
- ^ "Pesticide Exposure and Risk of Rheumatoid Arthritis among Licensed Male Pesticide Applicators in the Agricultural Health Study". Environmental Health Perspectives. 125 (7): 077010. July 2017. doi:10.1289/EHP1013. PMC 5744649 $2. PMID 28718769.
- ^ "Association between Vitamin D Deficiency and Antinuclear Antibodies in Middle-Aged and Older U.S. Adults". Cancer Epidemiology, Biomarkers & Prevention. 25 (12): 1559-1563. December 2016. doi:10.1158/1055-9965.EPI-16-0339. PMC 5135624 $2. PMID 27543618.
- ^ "Mechanisms for the induction of autoimmunity by infectious agents". The Journal of Clinical Investigation. 108 (8): 1097-104. October 2001. doi:10.1172/JCI14235. PMC 209539 $2. PMID 11602615.
- ^ "High risk of autoimmune diseases after COVID-19". Nature Reviews Rheumatology: 1-2. April 2023. doi:10.1038/s41584-023-00964-y. PMC 10096101 $2. PMID 37046064.
- ^ "Immune-mediated disease genetics: the shared basis of pathogenesis". Trends in Immunology. 34 (1): 22-6. January 2013. doi:10.1016/j.it.2012.09.001. PMID 23031829.
- ^ Harrison's Principles of Internal Medicine. 18th (İngilizce). 1–2. McGraw-Hill Professional. 11 Ağustos 2011. ISBN 978-0-07-174889-6.
- ^ Chang (December 2021). "New-onset IgG autoantibodies in hospitalized patients with COVID-19". Nature Communications. 12 (1): 5417. doi:10.1038/s41467-021-25509-3. PMC 8440763 $2. PMID 34521836.
- ^ "Chronic thyroiditis and autoimmunization". Journal of the American Medical Association. 164 (13): 1439-47. July 1957. doi:10.1001/jama.1957.02980130015004. PMID 13448890.
- ^ a b "Defining criteria for autoimmune diseases (Witebsky's postulates revisited)". Immunology Today. 14 (9): 426-30. September 1993. doi:10.1016/0167-5699(93)90244-F. PMID 8216719.
- ^ "Antinuclear Antibody (ANA)". labtestsonline.org. 22 Aralık 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 14 Nisan 2020.
- ^ "Complete blood count (CBC)". www.mayoclinic.org. 19 Aralık 2018. 22 Aralık 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 14 Nisan 2020.
- ^ MedlinePlus Medical Encyclopedia."Autoimmune disorders". MedlinePlus Medical Encyclopedia. U.S. National Library of Medicine. 2016-01-12. Archived from the original on 2016-01-12. Retrieved 2020-04-14.
- ^ "Drugs for Autoimmune Inflammatory Diseases: From Small Molecule Compounds to Anti-TNF Biologics". Frontiers in Pharmacology (İngilizce). 8: 460. 2017. doi:10.3389/fphar.2017.00460. PMC 5506195 $2. PMID 28785220.
- ^ a b c "Treating human autoimmunity: current practice and future prospects". Science Translational Medicine. 4 (125): 125sr1. March 2012. doi:10.1126/scitranslmed.3003504. PMC 4061980 $2. PMID 22422994.
- ^ a b c "Restoring the balance: immunotherapeutic combinations for autoimmune disease". Disease Models & Mechanisms. 7 (5): 503-13. May 2014. doi:10.1242/dmm.015099. PMC 4007402 $2. PMID 24795433.
- ^ "Epidemiology and estimated population burden of selected autoimmune diseases in the United States". Clinical Immunology and Immunopathology. 84 (3): 223-43. September 1997. doi:10.1006/clin.1997.4412. PMID 9281381.
- ^ a b "Updated assessment of the prevalence, spectrum and case definition of autoimmune disease". Autoimmunity Reviews. 11 (10): 754-65. August 2012. doi:10.1016/j.autrev.2012.02.001. PMID 22387972.
- ^ Dinse (June 2020). "Increasing Prevalence of Antinuclear Antibodies in the United States". Arthritis & Rheumatology (İngilizce). 72 (6): 1026-1035. doi:10.1002/art.41214. ISSN 2326-5191. PMC 7255943 $2. PMID 32266792.
- ^ "PPAR-delta senses and orchestrates clearance of apoptotic cells to promote tolerance". Nature Medicine. 15 (11): 1266-72. November 2009. doi:10.1038/nm.2048. PMC 2783696 $2. PMID 19838202.
- ^ "Autoimmune kidney disease and impaired engulfment of apoptotic cells in mice with macrophage peroxisome proliferator-activated receptor gamma or retinoid X receptor alpha deficiency". Journal of Immunology. 186 (1): 621-31. January 2011. doi:10.4049/jimmunol.1002230. PMC 4038038 $2. PMID 21135166.
- ^ "Genes, tolerance and systemic autoimmunity". Autoimmunity Reviews. 11 (9): 664-9. July 2012. doi:10.1016/j.autrev.2011.11.017. PMC 3306516 $2. PMID 22155015.
- ^ "Disruption of the cytoskeleton after apoptosis induction with autoantibodies". Autoimmunity. 36 (3): 183-9. May 2003. doi:10.1080/0891693031000105617. PMID 12911286.
- ^ "Haematopoietic stem cell transplantation for autoimmune diseases". Nature Reviews. Rheumatology. 13 (4): 244-256. April 2017. doi:10.1038/nrrheum.2017.7. PMID 28228650.
- ^ "How stem cells could fix type 1 diabetes". Nature (İngilizce). 595 (7867): S64-S66. 14 Temmuz 2021. doi:10.1038/d41586-021-01842-x. PMID 34262205. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Glycans in the immune system and The Altered Glycan Theory of Autoimmunity: a critical review". Journal of Autoimmunity. 57: 1-13. February 2015. doi:10.1016/j.jaut.2014.12.002. PMC 4340844 $2. PMID 25578468.
- ^ "Hygiene hypothesis and autoimmune diseases". Clinical Reviews in Allergy & Immunology. 42 (1): 5-15. February 2012. doi:10.1007/s12016-011-8285-8. PMID 22090147.
- ^ a b c d e f g Harrison (January 2020). "Vitamin D, Autoimmune Disease and Rheumatoid Arthritis". Calcified Tissue International (İngilizce). 106 (1): 58-75. doi:10.1007/s00223-019-00577-2. ISSN 0171-967X. PMC 6960236 $2. PMID 31286174.
- ^ a b Lucas (12 Ağustos 2018). "On the Nature of Evidence and 'Proving' Causality: Smoking and Lung Cancer vs. Sun Exposure, Vitamin D and Multiple Sclerosis". International Journal of Environmental Research and Public Health. 15 (8): 1726. doi:10.3390/ijerph15081726. PMC 6121485 $2. PMID 30103527.
