Prosiyanidin

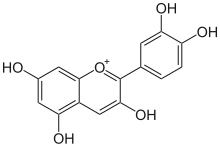
Prosiyanidinler, flavonoidler sınıfına ait proantosiyanidinlerin (veya yoğunlaştırılmış tanenlerin) üyeleridir. Kateşin ve epikateşin moleküllerinden oluşan oligomerik bileşiklerdir. Oksidatif koşullar altında depolimerize edildiklerinde siyanidin üretirler.
Bitkilerde Dağılımı
[değiştir | kaynağı değiştir]Prosiyanidinler, daha az biyoaktif/biyoyararlı polimerler (4 veya daha fazla kateşin) dahil olmak üzere, birçok bitkide bulunan yoğunlaştırılmış bir flavan-3-ol grubunu temsil eder ve en çok elma, sahil çamı kabuğu, tarçın, aronya meyvesi, kakao çekirdekleri, üzüm çekirdeği, üzüm kabuğu[1] ve Vitis vinifera (sıradan üzüm) kırmızı şaraplarında bulunur.[2] Bununla birlikte, yaban mersini, kızılcık, siyah frenk üzümü, yeşil çay, siyah çay ve diğer bitkiler de bu flavonoidleri içerir.[3] Prosiyanidinler ayrıca Quercus petraea ve Q. robur öz odunundan (şarap fıçısı meşeleri) da izole edilebilir.[4] Açaí palmiyesinin ( Euterpe oleracea) meyvesinden elde edilen Açaí yağı, çok sayıda prosiyanidin oligomeri bakımından zengindir.[5]
Elmalar, porsiyon başına şarapta bulunan prosiyanidin miktarının ortalama sekiz katı miktarını içerir; en yüksek miktarlar ise Kırmızı elma ve Yeşil elma çeşitlerinde bulunur.[6]
Tarla baklasının (Vicia faba) [7] tohum kabukları, domuz yavrularında [8] sindirimi etkileyen ve enzimler [9] üzerinde inhibe edici etkisi olabilen prosiyanidinler içerir. Aynı zamanda, Cistus salviifolius de oligomerik prosiyanidinler içerir.[10]
Analiz
[değiştir | kaynağı değiştir]Kondanse tanenler, depolimerizasyon, asimetrik akış alan akışı fraksiyonlaması veya küçük açılı X-ışını saçılması dahil olmak üzere çeşitli tekniklerle karakterize edilebilir. DMACA, bitki histolojisinde prosiyanidin bileşiklerinin lokalizasyonu için kullanılan bir boyadır. Reaktifin kullanımı mavi boyanmaya neden olur.[11] Prosiyanidinleri titre etmek için de kullanılabilir. Toplam fenoller (veya antioksidan etkisi) Folin-Ciocalteu reaksiyonu kullanılarak ölçülebilir. Sonuçlar tipik olarak gallik asit eşdeğerleri (GAE) olarak ifade edilir.
Tarla fasulyesi (Vicia faba)[12] veya arpadan [13] elde edilen prosiyanidinler, kateşin veya proantosiyanidinlerin varlığında testte kırmızı bir renk oluşmasına neden olan vanilin-HCl yöntemi kullanılarak tahmin edilmiştir.
Prosiyanidinler, Prosiyanidolik İndeks (Bates-Smith Tahlili olarak da adlandırılır) kullanılarak titre edilebilir. Ürünün belirli kimyasallarla karıştırıldığında renk değişimini ölçen bir test yöntemidir. Renk değişimi ne kadar büyük olursa, PCO içeriği de o kadar yüksek olur. Ancak, Prosiyanidolik İndeks, 100'ün üzerinde iyi ölçüm yapabilen göreli bir değerdir. Ne yazık ki, 95'lik bir Prosiyanidolik İndeks bazıları tarafından hatalı bir şekilde %95 PCO olarak algılanmış ve bitmiş ürünlerin etiketlerinde görünmeye başlamıştır. Mevcut tüm analiz yöntemleri, bu ürünlerin gerçek PCO içeriğinin %95'ten çok daha düşük olduğunu göstermektedir.[14]
Porter Tahlili veya butanol-HCl-demir yöntemi olarak adlandırılan geliştirilmiş bir kolorimetrik test, şu anda en yaygın kullanılan PCO tahlilidir.[15] Porter Tahlili'nin ölçüm birimi PVU'dur (Porter Değer Birimi). Porter Tahlili, üzüm çekirdeği ekstraktı gibi prosiyanidin içeren bileşiklerin gücünü belirlemeye yardımcı olan kimyasal bir testtir. Daha büyük zincir birimlerini (dimerler ve trimerler) tek birim monomerlere ayıran ve oksitleyen bir asit hidrolizidir. Bu, bir spektrofotometre kullanılarak ölçülebilen bir renk değişikliğine yol açar. Belirli bir ışık dalga boyunda absorbans ne kadar yüksek olursa, güç de o kadar yüksek olur. Üzüm çekirdeği ekstraktı için aralıklar, düşük kaliteli malzeme için 25 PVU'dan birinci sınıf üzüm çekirdeği ekstraktları için 300'ün üzerine kadar değişir.[16]
Jel geçirgenlik kromatografisi (GPC) analizi, monomerlerin daha büyük PCO moleküllerinden ayrılmasını sağlar.
Prosiyanidin monomerleri, HPLC analizi ile karakterize edilebilir. Kondanse tanenler, floroglusinol (floroglusinoliz olarak adlandırılan reaksiyon), tiyoglikolik asit (tiyoglikoliz), benzil merkaptan veya sisteamin (tiyoliz olarak adlandırılan işlemler[17]) gibi bir nükleofil varlığında asit katalizli bölünmeye uğrayabilir ve daha sonra analiz edilebilen oligomerlerin oluşumuna yol açar.[18]
Floroglusinoliz, örneğin şarap[19] veya üzüm çekirdeği ve kabuk dokularında[20] prosiyanidinlerin karakterizasyonu için kullanılabilir.
Tiyoglikoliz, prosiyanidinleri[21] veya kondanse tanenlerin oksidasyonunu[22] incelemek için kullanılabilir. Lignin kantitasyonu için de kullanılır.[23] Douglas köknar kabuğundan elde edilen kondanse tanenler üzerindeki reaksiyon, epikateşin ve kateşin tiyoglikolatları üretir.[24]
Lithocarpus glaber yapraklarından elde edilen kondanse tanenler, sisteamin varlığında asit katalizli bozunma yoluyla analiz edilmiştir.[25]
Araştırma
[değiştir | kaynağı değiştir]Besin takviyelerindeki prosiyanidin içeriği yeterince belgelenmemiştir.[26] Pirenol, %70 prosiyanidin içeren ve sahil çamı kabuğu özlerinden elde edilen bir besin takviyesidir ve birçok rahatsızlığı tedavi edebileceği iddialarıyla pazarlanmaktadır. Ancak, yedi farklı kronik rahatsızlığın tedavisinde kullanımını destekleyecek yeterli tıbbi kanıt bulunmamaktadır.[27]
Ayrıca bakınız
[değiştir | kaynağı değiştir]Kaynakça
[değiştir | kaynağı değiştir]- ^ Souquet, J; Cheynier, Véronique; Brossaud, Franck; Moutounet, Michel (1996). "Polymeric proanthocyanidins from grape skins". Phytochemistry. 43 (2). ss. 509-512. doi:10.1016/0031-9422(96)00301-9.
- ^ Yang, J; Xiao, YY (2013). "Grape phytochemicals and associated health benefits". Crit Rev Food Sci Nutr. 53 (11). ss. 1202-1225. doi:10.1080/10408398.2012.692408. PMID 24007424.
- ^ USDA, August 2004. USDA Database for the Proanthocyanidin Content of Selected Foods. PDF summary accessed from main USDA page here. Page accessed July 31, 2015
- ^ Vivas, N; Nonier, M; Pianet, I; Vivasdegaulejac, N; Fouquet, E (2006). "Proanthocyanidins from Quercus petraea and Q. robur heartwood: quantification and structures". Comptes Rendus Chimie. Cilt 9. ss. 120-126. doi:10.1016/j.crci.2005.09.001.
- ^ Pacheco-Palencia LA, Mertens-Talcott S, Talcott ST (Jun 2008). "Chemical composition, antioxidant properties, and thermal stability of a phytochemical enriched oil from Acai (Euterpe oleracea Mart.)". J Agric Food Chem. 56 (12). ss. 4631-4636. doi:10.1021/jf800161u. PMID 18522407.
- ^ Hammerstone, John F.; Lazarus, Sheryl A.; Schmitz, Harold H. (August 2000). "Procyanidin content and variation in some commonly consumed foods". The Journal of Nutrition. 130 (8S Suppl). ss. 2086S-92S. doi:10.1093/jn/130.8.2086S. PMID 10917927.
Figure 5
Geçersiz|doi-access=free(yardım) - ^ Merghem, R.; Jay, M.; Brun, N.; Voirin, B. (2004). "Qualitative analysis and HPLC isolation and identification of procyanidins fromvicia faba". Phytochemical Analysis. 15 (2). ss. 95-99. doi:10.1002/pca.731. PMID 15116939.
- ^ Van Der Poel, A. F. B.; Dellaert, L. M. W.; Van Norel, A.; Helsper, J. P. F. G. (2007). "The digestibility in piglets of faba bean (Vicia faba L.) as affected by breeding towards the absence of condensed tannins". British Journal of Nutrition. 68 (3). ss. 793-800. doi:10.1079/BJN19920134. PMID 1493141. Geçersiz
|doi-access=free(yardım) - ^ Griffiths, D. W. (1981). "The polyphenolic content and enzyme inhibitory activity of testas from bean (Vicia faba) and pea (Pisum spp.) varieties". Journal of the Science of Food and Agriculture. 32 (8). ss. 797-804. doi:10.1002/jsfa.2740320808.
- ^ Qa’Dan, F.; Petereit, F.; Mansoor, K.; Nahrstedt, A. (2006). "Antioxidant oligomeric proanthocyanidins fromCistus salvifolius". Natural Product Research. 20 (13). ss. 1216-1224. doi:10.1080/14786410600899225. PMID 17127512.
- ^ Bogs, J.; Jaffe, F. W.; Takos, A. M.; Walker, A. R.; Robinson, S. P. (2007). "The Grapevine Transcription Factor VvMYBPA1 Regulates Proanthocyanidin Synthesis during Fruit Development". Plant Physiology. 143 (3). ss. 1347-1361. doi:10.1104/pp.106.093203. PMC 1820911 $2. PMID 17208963.
- ^ Cabrera, A.; Martin, A. (2009). "Genetics of tannin content and its relationship with flower and testa colours in Vicia faba". The Journal of Agricultural Science. Cilt 113. ss. 93-98. doi:10.1017/S0021859600084665.
- ^ Kristensen, H.; Aastrup, S. (1986). "A non-destructive screening method for proanthocyanidin-free barley mutants". Carlsberg Research Communications. 51 (7). ss. 509-513. doi:10.1007/BF02906893. Geçersiz
|doi-access=free(yardım) - ^ Grape Seed Extract, White paper, The Grape Seed Method Evaluation Committee, Under the Auspices of NNFA ComPli 24 Aralık 2002 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ The Truth About PCOs, Debasis Bagchi, Ph.D. on www.activin.com 19 Ekim 2013 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Porter Assay on www.omegabiotech.com
- ^ Torres, J. L.; Lozano, C. (2001). "Chromatographic characterization of proanthocyanidins after thiolysis with cysteamine". Chromatographia. 54 (7–8). ss. 523-526. doi:10.1007/BF02491211.
- ^ Jorgensen, Emily M.; Marin, Anna B.; Kennedy, James A. (2004). "Analysis of the Oxidative Degradation of Proanthocyanidins under Basic Conditions". Journal of Agricultural and Food Chemistry. 52 (8). ss. 2292-2296. doi:10.1021/jf035311i. PMID 15080635.
- ^ Analysis of Tannins in Red Wine Using Multiple Methods: Correlation with Perceived Astringency by mean of depolymerisation James A. Kennedy, Jordan Ferrier, James F. Harbertson and Catherine Peyrot des Gachons, Am. J. Enol. Vitic. 57:4, 2006, pp. 481–485
- ^ Kennedy, J. A.; Jones, G. P. (2001). "Analysis of Proanthocyanidin Cleavage Products Following Acid-Catalysis in the Presence of Excess Phloroglucinol". Journal of Agricultural and Food Chemistry. 49 (4). ss. 1740-1746. doi:10.1021/jf001030o. PMID 11308320.
- ^ Sears, K. D.; Casebier, R. L. (1968). "Cleavage of proanthocyanidins with thioglycollic acid". Chemical Communications, 22. s. 1437. doi:10.1039/C19680001437.
- ^ Vernhet, A.; Dubascoux, S. P.; Cabane, B.; Fulcrand, H. L. N.; Dubreucq, E.; Poncet-Legrand, C. L. (2011). "Characterization of oxidized tannins: Comparison of depolymerization methods, asymmetric flow field-flow fractionation and small-angle X-ray scattering". Analytical and Bioanalytical Chemistry. 401 (5). ss. 1559-1569. doi:10.1007/s00216-011-5076-2. PMID 21573842. Vernhet, A.; Dubascoux, S. P.; Cabane, B.; Fulcrand, H. L. N.; Dubreucq, E.; Poncet-Legrand, C. L. (2011). "Characterization of oxidized tannins: Comparison of depolymerization methods, asymmetric flow field-flow fractionation and small-angle X-ray scattering". Analytical and Bioanalytical Chemistry. 401 (5). ss. 1559-1569. doi:10.1007/s00216-011-5076-2. PMID 21573842.
- ^ Lange, B. M.; Lapierre, C.; Sandermann Jr, H. (1995). "Elicitor-Induced Spruce Stress Lignin (Structural Similarity to Early Developmental Lignins)". Plant Physiology. 108 (3). ss. 1277-1287. doi:10.1104/pp.108.3.1277. PMC 157483 $2. PMID 12228544.
- ^ Douglas-Fir Bark: Characterization of a Condensed Tannin Extract, by Hong-Keun Song, A thesis submitted to Oregon State University in partial fulfillment of the requirements for the degree of Master of Science, December 13, 1984
- ^ Zhang, L. L.; Lin, Y. M. (2008). "HPLC, NMR and MALDI-TOF MS Analysis of Condensed Tannins from Lithocarpus glaber Leaves with Potent Free Radical Scavenging Activity". Molecules. 13 (12). ss. 2986-2997. doi:10.3390/molecules13122986. PMC 6245341 $2. PMID 19052523. Geçersiz
|doi-access=free(yardım) - ^ USDA Database for the Proanthocyanidin Content of Selected Foods (PDF). August 2004. 16 Ekim 2010 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 9 Ocak 2013.[sayfa belirt]
- ^ Robertson, Nina U.; Schoonees, Anel; Brand, Amanda; Visser, Janicke (29 Eylül 2020). "Pine bark (Pinus spp.) extract for treating chronic disorders". The Cochrane Database of Systematic Reviews. 2020 (9). ss. CD008294. doi:10.1002/14651858.CD008294.pub5. ISSN 1469-493X. PMC 8094515 $2. PMID 32990945.
