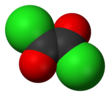
Okzalil klorür
Görünüm
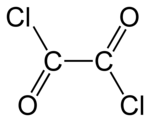
| |||
| |||

| |||
| Adlandırmalar | |||
|---|---|---|---|
Tercih edilen IUPAC adı Okzalil diklorür[1] | |||
Etandioil diklorür[1] | |||
Diğer adlar
| |||
| Tanımlayıcılar | |||
3D model (JSmol)
|
|||
| ChemSpider | |||
| ECHA InfoCard | 100.001.092 | ||
| EC Numarası |
| ||
PubChem CID
|
|||
| RTECS numarası |
| ||
| UNII | |||
CompTox Bilgi Panosu (EPA)
|
|||
| |||
| |||
| Özellikler | |||
| Kimyasal formül | C2Cl2O2 | ||
| Molekül kütlesi | 126,93 g mol−1 | ||
| Görünüm | renksiz sıvı | ||
| Koku | fosgen benzeri | ||
| Yoğunluk | 1,4785 g/mL | ||
| Erime noktası | -16 °C (3 °F; 257 K) | ||
| Kaynama noktası | 63 ila 64 °C (145 ila 147 °F; 336 ila 337 K) 1.017 bar | ||
| Çözünürlük (su içinde) | tepkir | ||
| Kırınım dizimi (nD) | 1,429 | ||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | Zehirli, korozif, gözyaşartıcı[2] | ||
| GHS etiketleme sistemi: | |||
| Piktogramlar |   [2] [2]
| ||
| İşaret sözcüğü | Danger[2] | ||
| Tehlike ifadeleri | H314, H331[2] | ||
| Önlem ifadeleri | P261, P280, P305+P351+P338, P310[2] | ||
| NFPA 704 (yangın karosu) |
|||
| Güvenlik bilgi formu (SDS) | External MSDS | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |||
| Bilgi kutusu kaynakları | |||
Okzalil klorür, (COCl)2 formüllü kimyasal bileşik. Keskin kokulu, renksiz sıvıdır. Okzalik asitin açil klorürüdür. 61 °C'de kaynar. Zehirlidir ve suyla tepkimeye girerek hidrojen klorür, karbonmonoksit ve karbon dioksit gazlarını verir.
İlk olarak 1892'de Fransız kimyager Adrien Fauconnier tarafından dietil okzalat ile fosfor pentaklorürün tepkimesi sonucu elde edilmiştir.
Kaynakça
[değiştir | kaynağı değiştir]| Organik kimya ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. |
- ^ a b Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. s. 797. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ^ a b c d e Oxalyl chloride MSDS